生成AIが設計した薬が世界初フェーズ3へ——2026年は「AIドラッグ元年」になるか
AI創薬の歴史に、一つの区切りが刻まれた。
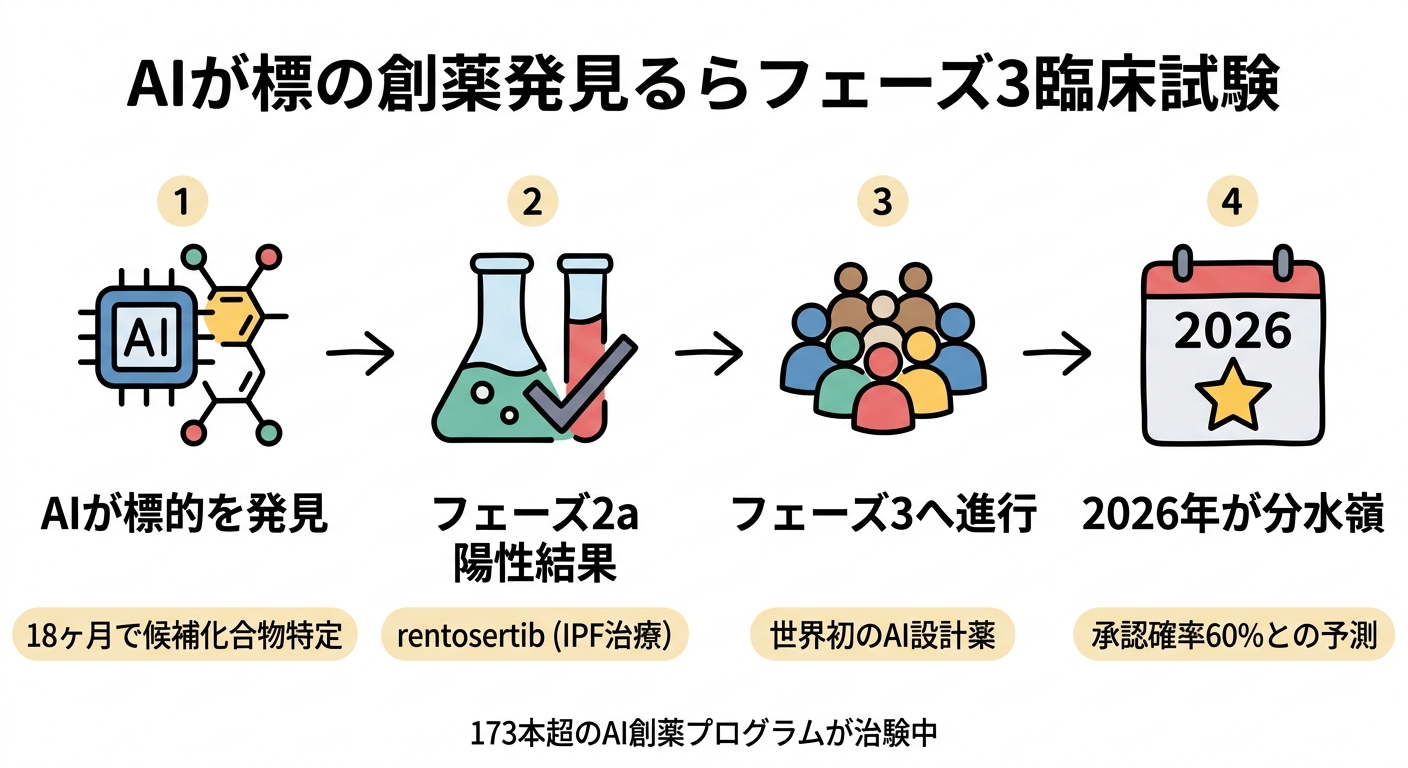
香港発のバイオテック企業Insilico Medicineが開発した「rentosertib」が、フェーズ2a試験で陽性結果を出し、フェーズ3への進行が決まった。AIが分子レベルから設計し、ターゲット発見から候補化合物の最適化まで一貫してAIが担った薬が、大規模な臨床試験に到達したのは世界初のことだ。
率直に言えば、この一件だけで「AI創薬の時代が来た」と叫ぶのは早計だ。しかしそれ以上に、173本を超えるAI創薬プログラムが現在治験中であり、そのうち15〜20本が2026年中にフェーズ3入りを予定しているという数字は、単なる話題ではない。製薬業界の構造変化が、数字として見えてきている。
rentosertibとは何か
対象疾患は特発性肺線維症(IPF)だ。肺組織が徐々に硬くなり、呼吸機能が低下していく難病で、現在の標準治療では進行を遅らせることはできても根本的な治療には至っていない。
rentosertibが狙うのは「TNIK」というタンパク質だ。Insilico Medicineは自社開発のAIプラットフォーム「Pharma.AI」を使い、ヒトゲノムデータと疾患関連データを解析。TNIKをIPFの新規治療標的として特定し、そこに結合する低分子化合物をAIで設計した。
通常、ターゲット発見から候補化合物の特定まで5〜10年を要するとされるプロセスを、Insilicoは18ヶ月に圧縮したと主張している。フェーズ2aでは安全性と予備的有効性が確認され、次のフェーズ3では有効性の本格検証に入る。
「完全循環型創薬」という新しい図式
ここで気になるのは、rentosertibが持つ象徴的な意味合いだ。
従来の創薬では、研究者が文献や実験データを積み重ね、標的分子を仮説として立て、化合物ライブラリを手作業でスクリーニングしていた。AIはその一部——たとえば化合物の構造最適化だけ——に使われることが多かった。
Insilicoが打ち出しているのはそれとは異なるモデルだ。「標的発見→化合物設計→毒性予測→治験計画」まで、AIが各ステップを担う完全循環型の創薬プロセスだ。これが現実になるとすれば、新薬開発の時間軸とコスト構造が根本から変わる。現在1,000億円超とも言われる新薬一本あたりの開発費が、どこまで圧縮できるのか。
2026年が「分水嶺」と言われる理由
Nature Medicineに掲載された分析によれば、現在173本超のAI関連創薬プログラムが何らかの段階の治験に入っている。そのうち2026年中にフェーズ3へ進む見込みのものが15〜20本とされる。
フェーズ3は最終関門だ。数百から数千人規模の患者を対象に、プラセボや既存治療薬との比較試験を行う。費用は数百億円単位になることもあり、ここで失敗すれば承認申請には至らない。逆に言えば、フェーズ3への進行は「動物実験や小規模臨床では見えなかったものが、大規模で検証される段階に来た」ことを意味する。
2026〜27年中に初のAI設計薬が承認される確率は「約60%」という見方もある。この数字をどう読むかは人によって違うだろうが、個人的には思ったより高い確率だと感じた。製薬の世界では候補化合物の承認確率は全体で10〜12%とされており、フェーズ3に到達した段階でも50〜60%とされている。AI設計薬が既存の統計と同程度の水準にあるとすれば、それ自体が驚きだ。
既存製薬会社はどう動いているか
スタートアップだけの話ではない。
ファイザー、ノバルティス、アストラゼネカ、エーザイといった大手製薬各社が、AI創薬スタートアップとの提携や自社開発を加速している。Exscientia(英国)、Recursion Pharmaceuticals(米国)、Absci(米国)など、AI創薬を主軸に置く企業が相次ぎ上場・資金調達を果たしており、2025年だけで業界全体に数十億ドル規模の投資が流入した。
既存の製薬大手が警戒しているのは、「開発スピード」の非対称性だ。AIを使うスタートアップが候補化合物を2〜3年で臨床試験まで持ち込めるなら、10年サイクルで動く大手の競争優位は失われかねない。製薬大手がAIスタートアップを買収・提携する動きが急ピッチなのは、そのためだ。
解決されていない問題
もちろん、楽観論だけでは補えない部分もある。
まず、「AIが設計した」という定義自体が曖昧になりつつある。化合物の初期スクリーニングにAIを使っただけのプログラムも「AI創薬」として計上されるケースがあり、数字の膨張が起きている可能性がある。173本という数字のうち、どれだけが「本当の意味でAIが主導した」ものかは精査が必要だ。
次に、フェーズ3以降の問題がある。承認されたとして、その薬が実際に患者に届くまでには薬価交渉、製造体制の確立、医師への普及教育が必要だ。AIが開発を速めても、社会実装のボトルネックは依然として人間側にある。
さらに、AIモデルの「解釈可能性」の問題もある。AIがなぜその化合物を設計したかを人間が完全に理解できない場合、規制当局が承認審査で何を根拠とするかが問われてくる。FDAは既にAI/MLを使った医薬品開発への対応方針を検討中だが、具体的な枠組みは固まっていない。
製薬産業の地殻変動
rentosertibのフェーズ3進行は、AI創薬が「研究室の話題」から「規制と市場の現実」に踏み込んだことを示すシンボルだ。
製薬産業の歴史では、コンビナトリアルケミストリーの台頭(1990年代)、ゲノム解析の実用化(2000年代)、生物製剤の拡大(2010年代)と、技術革新が節目ごとに業界の構造を変えてきた。AI創薬がその次の節目になるかどうか、2026〜27年の臨床試験結果が重要な答えを出す。
承認が出れば「AIドラッグ元年」として記録されるだろう。出なければ、AI創薬への投資熱は一時的に冷える可能性がある。どちらに転ぶにせよ、この数年が製薬業界にとって決定的な時期になることは間違いない。
Sources:
- AI-Discovered Drugs Reach Phase III and 2026 Will Determine Whether All the Promises Were Real | HumAI Blog
- AI in drug discovery: from target identification to clinical trials | Nature Medicine
- Insilico Medicine Announces Positive Phase 2a Results for rentosertib | Insilico Medicine Blog
